ASCO LBA重磅发布:全球首个靶免巩固治疗Ⅲ期非小细胞肺癌研究,中位PFS突破15个月刷新记录

约1/3的非小细胞肺癌(NSCLC)患者在首次确诊时已是III期,然而临床公认的免疫巩固治疗仍然获益有限,亟需探索更加有效的治疗策略。作为全球首个在同步/序贯放化疗后未进展III期NSCLC领域使用靶免联合巩固治疗方案的研究,R-ALPS研究验证了正大天晴“得福组合”的临床获益,中位无进展生存期(PFS)达15.1个月,刷新该领域的PFS获益纪录。当地时间6月2日,该突破性研究成果在2025年美国临床肿瘤学会(ASCO)年会上,以LBA(Late-Breaking Abstract)形式全球首发。

(陈明教授在大会现场作报告)
机制创新:靶免联合重塑晚期NSCLC巩固治疗格局
2022年全球肺癌发病人数248万,中国发病人数106.1万,发病率和死亡率位居第一,其中NSCLC约占80%-85%,且新发人数呈上升趋势[1,2]。目前,局部晚期/不可切除的Ⅲ期NSCLC治疗手段有限,主要为同步/序贯放化疗后继续使用免疫单药进行巩固治疗[3,4]。
此前开展的ALTER0303研究证实,盐酸安罗替尼可同时延长晚期NSCLC患者的无进展生存时间(PFS)和总生存期(OS)[5]。盐酸安罗替尼已获批NSCLC、小细胞肺癌、软组织肉瘤、子宫内膜癌、甲状腺髓样癌、分化型甲状腺癌等适应症。贝莫苏拜单抗(PD-L1抑制剂),通过结合PD-1和B7.1(CD80)受体发挥负向免疫调节作用。在机制研究中,肿瘤血管异常会促进组织乏氧、乳酸增多,从而激活免疫抑制,抑制T细胞功能。抗血管生成药物则通过诱导血管正常化、降低免疫抑制而增强效应免疫细胞的浸润[6]。
基于此,正大天晴开展了R-ALPS研究——贝莫苏拜单抗联合或不联合安罗替尼用于同步/序贯放化疗后未进展的局部晚期、不可切除(III期)NSCLC的巩固治疗的随机、双盲、平行对照、多中心III期临床研究。
临床验证:III期研究期中分析告捷,中位PFS 15.1个月
R-ALPS研究[7]纳入经病理确诊、同步/序贯放化疗后未进展的、局部晚期/不可切除的III期非小细胞肺癌患者。截至2023年5月12日,共完成553例患者随机入组,试验组1(209例)为贝莫苏拜单抗联合安罗替尼治疗、试验组2(212例)为贝莫苏拜单抗联合安慰剂治疗、对照组(132例)为安慰剂治疗,中位随访时间为19.4个月。
主要研究结果[7]显示:
●试验组1:中位PFS 为15.1个月,对照组4.2个月(HR=0.49, 95%CI 0.36-0.66, P<0.001),疾病进展或死亡风险降低51%。
●试验组2:中位PFS 为9.7个月,对照组 4.2个月(HR=0.53,95% CI 0.39-0.72,P<0.0001),疾病进展或死亡风险降低47%。
●预设的亚组分析(包括是否吸烟、前序治疗方式为同步/序贯)显示与各试验组获益趋势一致。
●安全性方面,≥3级治疗相关不良事件发生率(48.8% vs. 29.4% vs. 19.7%)。
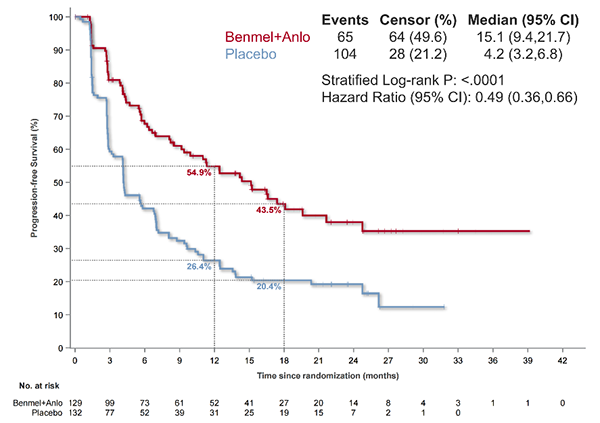
IRC评估的PFS(试验组1vs.对照组)
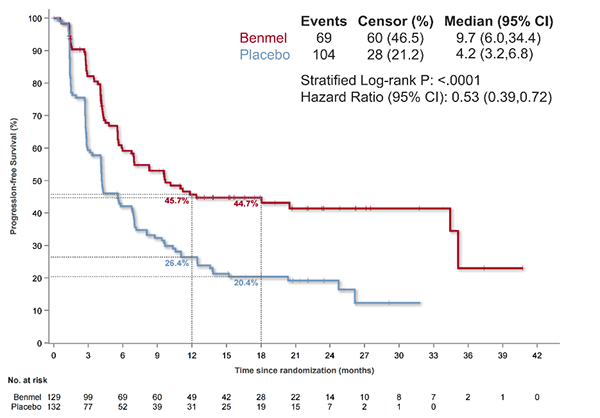
IRC评估的PFS(试验组2vs.对照组)
上市倒计时!“得福组合”巩固治疗方案上市申请获CDE受理
作为全球首个在同步/序贯放化疗后未进展III期NSCLC领域的联合用药研究,R-ALPS研究验证了靶免联合巩固治疗的有效性和安全性,标志着该治疗策略实现从机制创新到临床验证的关键跨越。
数据显示,相较于安慰剂治疗,贝莫苏拜单抗联合或不联合盐酸安罗替尼的新疗法,使同步/序贯放化疗后未进展的III期NSCLC患者中位PFS获益明显。基于该研究结果,贝莫苏拜联合或不联合盐酸安罗替尼胶囊的新适应症上市申请已于2025年4月由国家药品监督管理局药品审评中心(CDE)受理。该研究的突破性成果,可能重塑同步/序贯放化疗后未进展的III期NSCLC免疫单药维持治疗的临床实践指南,造福于更多NSCLC患者。

在不可切除III期NSCLC这一临床治疗高度复杂的领域,贝莫苏拜单抗联合安罗替尼作为放化疗后巩固治疗的III期临床研究取得重要突破,有望为全球肺癌诊疗增加新的选择。研究结果显示,贝莫苏拜联合安罗替尼方案的中位无进展生存期达15.1个月,疾病进展风险降低51%,创造了该领域无进展生存获益的最高纪录。特别值得关注的是,这一突破性疗效在各类预设亚组中均保持一致,包括不同吸烟状态和放化疗模式的患者群体,展现了该方案的广泛适用性。
通过靶免联合策略,研究设计既发挥了PD-L1抑制剂激活免疫系统的核心作用,又借助盐酸安罗替尼改善肿瘤微环境的协同效应,开创了放化疗后巩固治疗的新模式,体现了精准医学的理念。这种基于肿瘤生物学特性的联合干预,既符合肺癌多靶点干预的治疗趋势,也满足了临床对长程疗效维持的迫切需求。联合疗法获CDE受理预示着该创新疗法将为临床实践带来变革,标志着局部晚期NSCLC的维持治疗从单纯免疫激活,迈入“血管重塑-免疫协同”的新纪元。

虽然PACIFIC和GEMSTONE-301研究显示,同步或序贯放化疗后免疫巩固治疗可显著延长生存期,已成为该类患者的标准治疗。然而,大部分患者仍然在2年内出现肿瘤进展;部分患者,尤其是PD-L1表达低(<1%)的患者,免疫巩固治疗的获益有限。R-ALPS研究是首个评估免疫联合抗血管生成药物作为不可切除III期NSCLC放化疗后巩固治疗的III期随机试验,并取得了贝莫苏拜单抗联合安罗替尼组中位PFS为15.1个月,疾病进展风险降低51%的临床获益。此外,单药贝莫苏拜单抗也表现出PFS的临床获益,为患者提供了灵活的治疗选择,满足个体化治疗需求。
总的来说,R-ALPS研究为不可切除III期NSCLC的治疗开辟了新的道路,展现了免疫治疗与抗血管生成治疗联合的协同潜力。未来,我们期待更长时间的随访和总生存数据,以及对临床特征、生物标志物的深入探索,进一步明确这一联合策略的最佳获益人群,为III期NSCLC患者带来更显著的生存改善。

参考文献:
[1] Sung H, Ferlay J, Siegel RL, et al. Global Cancer Statistics 2020: GLOBOCAN Estimates of Incidence and Mortality Worldwide for 36 Cancers in 185 Countries. CA Cancer J Clin. 2021.
[2] Bray F, Laversanne M, Sung H, et al. Global cancer statistics 2022: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin. 2024.
[3] Antonia SJ, Villegas A, Daniel D, et al. Durvalumab after Chemoradiotherapy in Stage III Non-Small-Cell Lung Cancer. N Engl J Med. 2017;377(20):1919-1929.
[4] Qing Zhou,Ming Chen,et al.Sugemalimab versus placebo after concurrent or sequential chemoradiotherapy in patients with locally advanced, unresectable, stage III non-small-cell lung cancer in China (GEMSTONE-301): interim results of a randomised, double-blind, multicentre, phase 3 trial.The Lancet Oncology.2022;2(23).P209-219.
[5] Zhao Y, Wang Q, Zhang L, Shi J, Wang Z, Cheng Y, He J, Shi Y, Chen W, Luo Y, Wu L, Wang X, Nan K, Jin F, Dong J, Li B, Yamaguchi F, Breadner D, Nagano T, Tanaka F, Husain H, Li K, Han B. The efficacy of anlotinib as third-line treatment for non-small cell lung cancer by EGFR mutation status: a subgroup analysis of the ALTER0303 randomized phase 3 study. Transl Lung Cancer Res. 2022 May;11(5):776-785.
[6] Ramjiawan RR, Griffioen AW, Duda DG. Anti-angiogenesis for cancer revisited: Is there a role for combinations with immunotherapy.Angiogenesis. 2017;20(2):185-204.
[7]Ming Chen, Yongling Ji, Long Chen, et al. R-ALPS: A randomized, double-blind, placebo-controlled, multicenter phase III clinical trial of TQB2450 with or without anlotinib as maintenance treatment in patients with locally advanced and unresectable (stage III) NSCLC without progression following concurrent or sequential chemoradiotherapy.2025 ASCO(#LBA8004).
▲ 上下滑动查看更多
声明:
1.新闻稿旨在促进医药信息的沟通和交流,仅供医疗卫生专业人士参阅,非广告用途。
2.本公司不对任何药品和/或适应症作推荐。
3.本新闻稿中涉及的信息仅供参考,不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议。若您想了解具体疾病诊疗信息,请遵从医生或其他医疗卫生专业人士的意见或指导。
 简体中文
简体中文 English
English















